Sie befinden sich hier
Inhalt
Leitmuster zur ANA-Differenzierung
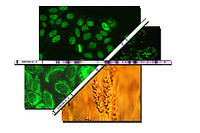
Für den Nachweis von Autoantikörpern gegen Gewebebestandteile oder Indikatorzellen, die auf Objektträgern immobilisiert sind, wird der indirekte Immunfluoreszenztest eingesetzt (iIFT).
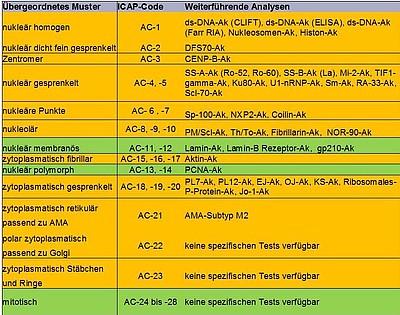
Die grundsätzliche Einteilung der im iIFT auf Hep-2 Zellen unterscheidbaren Muster(-typen) und einige der sie verursachenden Antigene bzw. zellulären Strukturen sind in der untenstehenden Tabelle zusammengefasst. Alle gelb unterlegten Bereiche sind Musterangaben die verpflichtend zu jedem im iIFT bestimmten Titer mitgeteilt werden müssen.
Hinweis: Streng genommen werden im ANA-Screening keine zytoplasmatischen Autoantikörper mit angegeben. Werden zytoplasmatische Fluoreszenzen als Nebenbefund bei den ANA ausgewiesen, ist eine eindeutige Kennzeichnung der Lokalisation des Fluoreszenzmusters (Nukleoplasma, Zytoplasma) unabdingbar.
Kommentar zur Stufendiagnostik Autoimmunserologie
Screening
ANA (antinukleäre AK, IgG, Reiter AutoAK)
Immunfluoreszenz-Test auf HEp-2 Zellen und Primatenleber. Geeignet zum Screening auf Autoantikörper, die mit systemischen Autoimmunerkrankungen assoziiert sind.
ENA-Pool (extrahierbare nukleäre Antigene; Reiter: Auto AK)
Bezeichnung für einen ELISA, der als Substrat ein Gemisch (Pool) aus sechs verschiedenen, klinisch relevanten Antigenen enthält. Ein negatives Ergebnis im ENA-Pool ELISA schließt das Vorliegen von Autoantikörpern nicht sicher aus. Der Begriff „ENA“ umreißt Autoantikörper, die eine größere Gruppe aus dem Zellkern extrahierbaren Antigenen binden. Die historisch bedingte Zuordnung wird heute allerdings für eine relativ fest umrissene Gruppe von Autoantigenen, zumeist nRNP/Sm, Sm, SS-A, SS-B, Scl-70, Jo-1 verwendet.
AMA (anti-mitochondriale AK)
Mitochondriale Autoantikörper sind gegen lysosomale Antigene oder Peroxisomen gerichtet. Der Nachweis von Autoantikörpern gegen mitochondriale Antigene erfolgt mittels Immunfluoreszenz auf einem geeigneten Substrat (Ratten-Niere). Das Ergebnis wird in Form einer Titerstufe angegeben. Der Cut off liegt hier bei einem Titer von 1:80. Ein deutlich positives Ergebnis (Titer >1:160) sollte durch die Bestimmung der Subspezifität AMA-M2 verifiziert werden. Das M2-Antigen enthält drei für die Autoimmunserologie relevante Epitope/Untereinheiten (E2-Untereinheiten im Pyruvatdehydrogenase-Komplex (PDC-E2), Branched-Chain-2-oxoacid-Dehydroenase-Komplex (BCOADC-E2) und 2-oxo-Glutarat-Dehydrogease-Komplex E (OGDC-E2)) und ist in Seren von Patienten mit primär biliärer Zirrhose (PBC) in etwa 90% der Fälle nachweisbar.
Anti-Neutrophilen-Zytoplasmatische Antikörper (ANCA)
Der Nachweis von Antikörpern gegen zytoplasmatische Antigene von neutrophilen Granulozyten (ANCA) erfolgt mittels Immunfluoreszenz-Tests auf humanen ethanol- oder formalin-fixierten Granulozyten.
In Abhängigkeit vom beobachteten Fluoreszenz-Muster unterscheidet man cANCA (wichtige Spezifität Proteinase-3, PR-3), pANCA (wichtige Spezifität Myeloperoxidase, MPO) oder atypische ANCA. Bei einem Screening-Ergebnis von 1:40 oder höher in der iIFT sollte eine Bestimmung von Proteinase-3 und/ oder MPO Antikörpern erfolgen. Bei pANCA positiven Seren treten neben der MPO-Spezifität auch Antikörper gegen Katalase, α-Enolase oder Lactoferrin auf. Der Nachweis dieser Spezifitäten ist i.d.R. aufgrund der geringen klinischen Relevanz nicht erforderlich.
Weiterführende Untersuchungen
ANA-Subspezifitäten als Einzelparameter
Hierbei untersucht man mittels eines Blot-Verfahrens Patientenseren auf das Vorliegen von Autoantikörpern gegen native Antigene/rekombinante Antigene.
LKM-AK (Leber-Nieren-Mikrosomen, LKM-1)
LKM-1 spezifische Antikörper binden an ein Protein der Cytochrom P450 Familie (Cyp 2D6). Sie kommen vor allem in Seren von Patienten mit Autoimmunhepatitis (Typ2) vor. Der Nachweis dieser Antikörperspezifität erfolgt mittels LineBlot Methodik. Das Ergebnis wird semi-quantiativ mitgeteilt.
SLA-AK (lösliches lebez. AG)
SLA Autoantikörper sind gegen bestimmte Bestandteile von Leber- oder Bauchspeicheldrüsenzellen gerichtet. Sie kommen vor allem bei Patienten mit autoimmuner Hepatitis oder Autoimmunerkrankungen mit Leberbeteiligung vor. Der Nachweis dieser Antikörper erfolgt mittels LineBlot. Das Ergebnis wird semi-quantiativ mitgeteilt.
SMA-AK (Glatte Muskulatur AK)
Gegen glatte Muskulatur gerichtete Antikörper werden mittels indirekter Immunfluoreszenz auf Magengewebe nachgewiesen. Diese Antikörper kommen bei Patienten mit autoimmuner chronisch-aktiver Hepatitis (Typ1) in 40-80% der Fälle vor, sind dann häufig gegen Aktin gerichtet und in höheren Titern nachweisbar. Ansonsten treten anti-SMA Antikörper auch bei Patienten mit primär biliärer Zirrhose (PBC, 10-20%) sowie Polymyositis (bis zu 30% der Fälle) auf.
Kontextspalte
Kontakt
Institut für Klinische Chemie
Haus 17 und Haus 22
Telefon 0621/383-2222
Telefax 0621/383-3912
ikc@umm.de
Auskünfte
Telefon 0621/383-2717
oder beim Bereichsleiter
oder wenn dringlich über den Arzt vom Dienst
Telefon 0621/383-1593