Sie befinden sich hier
Inhalt
Die präklinische Forschung ist ein Teilabschnitt der Erforschung neuer Behandlungsverfahren und geht der klinischen Forschung am Menschen voran. Ziel der Arbeitsgruppe ist es daher mithilfe experimenteller Modelle und der Darstellung von sowohl physiologischen, wie auch pathologischen Prozessen, neue Methoden und Wirkstoffe im Hinblick auf ein genau definiertes Behandlungsziel ermitteln zu können.
Die Forschungsschwerpunkte der seit 2007 bestehenden Arbeitsgruppe sind sowohl die MR- und CT-basierte Kleintierbildgebung, die experimentelle molekulare Bildgebung, sowie verschiedene Aspekte der Neuroonkologie. Besonders im Bereich der Bildgebung kooperiert die AG mit verschiedenen Forschungsgruppen (siehe Kooperationspartner).

Für die experimentelle und Kleintierbildgebung steht ein Volumen-CT (Yxlon Fox) zur Verfügung (Abb. 1).
Aufgrund einer flexiblen Positionierung des zu untersuchenden Objektes im Strahlengang ermöglicht das Gerät eine sehr hohe geometrische Vergrößerung. In Abhängigkeit von der Größe der Probe kann somit eine sehr hohe Auflösung bis in den einstelligen Mikrometerbereich erreicht werden. Die Kegelstrahlgeometrie des Strahlengangs erlaubt ein größeres Volumen mit nur einer Rotation des Objektes zu erfassen, wodurch die Akquisitionszeit deutlich reduziert wird.
Ein schnelles Untersuchungsprotokoll (sog. Quick Scan) kann CT-Aufnahmen innerhalb einer Untersuchungszeit von 33 Sekunden mit bis zu 1000 Projektionen akquirieren. Proportional kürzere Untersuchungszeiten sind bei reduzierter Anzahl an Projektionen möglich.
Ein Beispiel für die Bedeutsamkeit der präklinischen Bildgebung ist die Erforschung der Subarachnoidalblutung (SAB) mit ihren Folgen. Bei einer SAB kommt es spontan zu einer lebensbedrohlichen und sehr schmerzhaften Einblutung in den Subarachnoidalraum. Häufigste Ursache hierfür ist die Ruptur eines Aneurysmas. Im weiteren Verlauf der Erkrankung kommt es bei bis zu 70% der Patienten trotz initial erfolgreicher Behandlung der Blutungsquelle zu Verengungen der gehirnversorgenden Blutgefäße, sogenannte zerebralen Vasospasmen. Die Engstellung der Gefäße führt zu einer Minderperfusion und weiteren zerebralen Schäden, welche häufig mit bleibenden Schäden einhergehen oder tödlich enden.
Obwohl die SAB in Deutschland mit ca. 6400 Patienten jährlich ein relativ seltenes Krankheitsbild ist, so ist die Entwicklung neuer Behandlungsmethoden aufgrund der hohen Mortalität und verminderten Lebensqualität der Überlebenden unerlässlich.
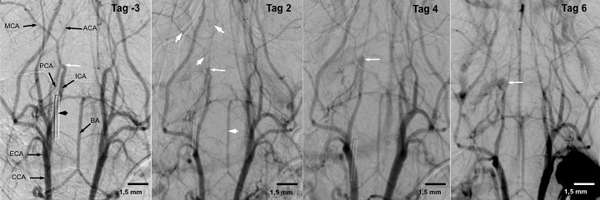
Beispielsweise besteht mit unserem Volumen-CT die Möglichkeit zur Durchführung von hochauflösenden digitalen Subtraktionsangiographien (DSA) der Hirngefäße bei Labornagern (Abb. 2). Durch diese Untersuchung können die Veränderungen im Durchmesser von zerebralen Gefäßen, den sog. Vasospasmen, nach experimentell ausgelöster Subarachnoidalblutung im longitudinalen Verlauf evaluiert werden. Im weiteren Verlauf besteht die Möglichkeit verschiedene Therapieansätze zu testen und deren Wirkungen zu erforschen.
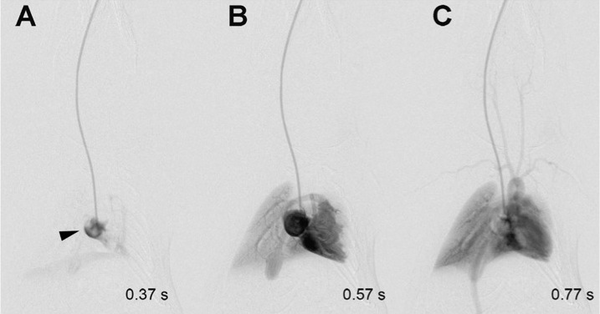
Darüber hinaus können auch digitale Subtraktionsangiographien im thorakalen und abdominalen Bereich angefertigt werden (Abb. 3).
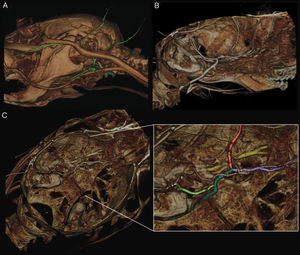
Eine weitere Option zur Darstellung der intrazerebralen Gefäße, ist die Verwendung des Quick Scans, um hochauflösende CT-Aufnahmen der Hirngefäße der Maus anzufertigen. (Abb. 4).
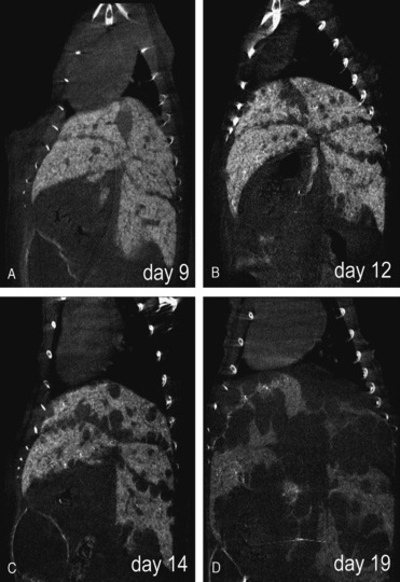
Neben Fragestellungen zum Gefäßstatus werden auch onkologische Fragestellungen bearbeitet, wie z.B. die Visualisierung von kleinsten Lebermetastasen bei Mäusen nach Applikation eines nanopartikulären Kontrastmittels (ExiTtron nano 6000; nanoPET Pharma GmbH, Berlin, Deutschland; Abb. 5).
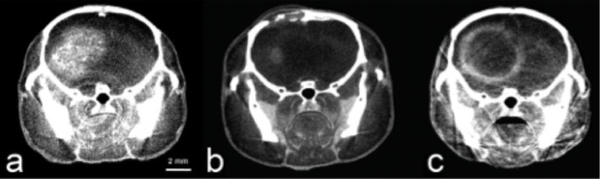
Auch intrazerebrale Tumore, wie zum Beispiel das Glioblastoma multiforme, lassen sich, nach Kontrastmittelapplikation (Iomeprol, Imeron 300) sehr gut darstellen (Abb. 6). Das Glioblastoma multiforme stellt mit 60% aller primären Tumore des zentralen Nervensystems den häufigsten malignen Tumor des Menschen dar. Unbehandelt liegt die durchschnittliche Überlebenszeit nach Diagnosestellung derzeit bei nur wenigen Monaten. Auch nach aggressiver Behandlung bestehend aus chirurgischer Tumorresektion, Strahlentherapie und ggf. Chemotherapie liegt die mittlere Überlebenszeit bei nur 15 Monaten.
Die chirurgische Tumorresektion ist oftmals durch die anatomische Lage des Tumors und seine makroskopisch nicht sichtbare Infiltration in das umgebende gesunde Hirngewebe unbefriedigend und der Tumor kann nur unvollständig entfernt werden. Dies limitiert die Erfolgsrate der chirurgischen Intervention erheblich und führt häufig zu Tumorrezidiven.
Die Strahlen- und Chemotherapie gehen neben ihrer unzureichenden Wirksamkeit mit zahlreichen Nebenwirkungen einher. Bei beiden Verfahren wird nicht nur das Tumorgewebe geschädigt, sondern auch gesundes Gewebe gerät in Mitleidenschaft.
Durch die präklinischen Bildgebung können Glioblastome und andere Tumorarten in ihrem longitudinalen Verlauf und hinsichtlich der Wirkung potenzieller neuer Wirkstoffe in Tiermodellen untersucht werden. Weiterhin besteht die Möglichkeit durch Kollimation des Kegelstrahls im Mikro-CT einen Nadelstrahl zu generieren, mit welchem eine punktgenaue Bestrahlung des Gehirns (Tumor) möglich ist (Abb. 6). Somit kann eine kombinierte Behandlung in Betracht gezogen werden.
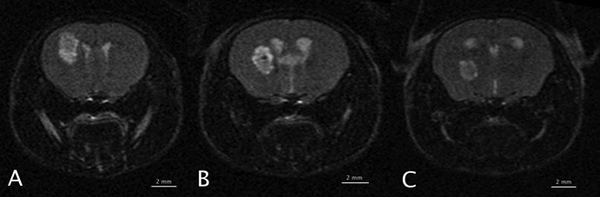
Neben dem Micro-CT hat die Arbeitsgruppe Zugriff auf ein modernes 1 Tesla Kleintier-MRT (Bruker BioSpec 94/20), welches sich besonders für die Darstellung von onkologischen Fragestellungen, wie zum Beispielt die Untersuchung von Glioblastomen (Abb. 7), eignet.
Ein weiterer Schwerpunkt der Arbeitsgruppe ist die ex vivo Bildgebung von humanen und tierischen Präparaten sowie diversen Medizinprodukten.
Beispielsweise können Stents für die Implantation im Menschen geprüft werden, um eventuelle Frakturen im Geflecht oder andere Beschädigungen auszuschließen. Das aus Metall bestehende Drahtgeflecht der traditionellen biokompatiblen Stents bietet hierbei einen hervorragenden Kontrast. Außerdem können Insekten, welche mit röntgenkontrastgebenden Substanzen eingefärbt wurden, hochauflösend dargestellt werden.
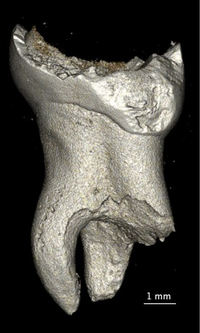
Ebenso ist die Untersuchung von bereits extrahierten Zähnen möglich, die aufgrund der unterschiedlichen Röntgendichten ihrer Strukturen eine Unterscheidung von Zahnschmelz, Dentin und Pulpahöhle ermöglichen. Des Weiteren können auch Mikrofissuren oder Zahnschmelzveränderungen sehr gut detektiert werden. Ein Beispiel ist die Erforschung von genetisch bedingten Veränderungen in der Zahnentwicklung: Abhängig vom Schweregrad der Zahnbildungsstörungen, müssen den betroffenen Patienten die Zähne vorzeitig extrahiert werden. Diese können im Anschluss in der Mikro-CT untersucht werden, um eventuell neue Erkenntnisse zu gewinnen (Abb. 8).
Die verschiedenen Bildgebungsmodalitäten erlauben bei minimaler Belastung der Tiere die longitudinale Evaluierung von Krankheitsprozessen und die Testung der Wirksamkeit neuer Medikamente, während gleichzeitig die Zahl der notwendigen Tiere reduziert werden kann. Ein wichtiger Aspekt, welcher eine große Rolle spielt, ist der Tierschutz und die Einhaltung des 3R Prinzips. Ziel des 3R Prinzips ist es Tierversuche zu vermeiden (Replacement), die Zahl der in Tierversuchen verwendeten Tiere zu reduzieren (Reduction) und ihr Leiden auf ein unerlässliches Maß zu beschränken (Refinement). Diese Richtlinien möchten wir jederzeit einhalten, um eine Balance zwischen der Notwendigkeit von Tierversuchen zum Zwecke des medizinische Fortschrittes und der Möglichkeit Tierversuche durch andere Methoden zu ersetzen, zu finden.
Kooperationspartner:
- Dr. med. Michael Ehmann, Klinik für Strahlentherapie und Radioonkologie, Universitätsmedizin Mannheim
- Prof. Dr. med. Dr. rer. nat. Lothar Schilling, Abteilung für Neurochirurgische Forschung, Universitätsmedizin Mannheim
- Prof. Dr. B. Wängler, Molekulare Bildgebung und Radiochemie, Klinik für Radiologie und Nuklearmedizin, Universitätsmedizin Mannheim
