Genetische Instabilität bei hämatologischen Erkrankungen
Leitung:
Priv.-Doz. Dr. rer. nat. Wolfgang Seifarth
Prof. Dr. rer. nat. Alice Fabarius
Leitung:
Priv.-Doz. Dr. rer. nat. Wolfgang Seifarth
Prof. Dr. rer. nat. Alice Fabarius
Chromosomale Instabilität (CIN) und klonale Evolution sind Kennzeichen aggressiver Malignome und zählen zu den größten Hindernissen für eine erfolgreiche Krebstherapie. Die mit CIN assoziierten Karyotypveränderungen (Aneuploidie) gehen klinisch in der Regel mit Therapieresistenz und Tumorprogression einher. Einer der Hauptursachen für die Entstehung aneuploider Tumorzellen ist die Fehlverteilung kompletter Chromosomen während der Zellteilung durch eine fehlerhafte mitotische Spindel, ausgelöst durch eine veränderte Anzahl von Polkörperchen (Zentrosomen).
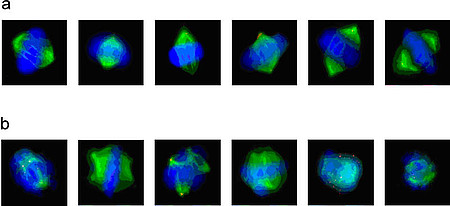
Dieser Zentrosomenamplifikation, speziell der Akkumulation zusätzlicher Zentrosomen (n>2), begegnet man nicht nur in Malignomen, sondern oft auch bereits in präneoplastischen Läsionen und frühen Stadien der Karzinogenese/Leukämogenese. Schlüsselenzym der Zellteilung und Zentrosomenverdopplung ist ESPL1/Separase, eine intrazelluläre Cystein-Endopeptidase. Seine strenge räumliche und zeitliche Regulation stellt sicher, dass die Erbinformation bei der Mitose gleichmäßig auf die entstehenden Tochterzellen verteilt wird und Zentrosomen während des Zellzyklus exakt einmal dupliziert werden. Überexpression oder eine vom Zellzyklus entkoppelte Separase-Überaktivität sind als Ursachen für Zentrosomenamplifikation, mitotische Spindeldefekte und Aneuploidy bekannt.
Bei der chronischen myeloischen Leukämie (CML) haben wir kürzlich Hinweise darauf gefunden, dass Separase-Überaktivität mit einer Beschleunigung des Krankheitsverlaufes assoziiert ist. Wir postulieren, dass bei dieser Erkrankung eine erhöhte Separaseaktivität in leukämischen Zellen die Entstehung neuer aneuploider Mutanten mit erhöhter Fähigkeit zur Therapieresistenz und klonaler Evolution begünstigt.
Unter Einsatz verschiedener Methoden, wie der konventionellen Zytogenetik, Durchflusszytometrie (FACS) sowie Zentrosomen-, Genexpressions- und DNA-Mutationsanalysen, arbeiten wir daran, die molekularen Mechanismen der oben genannten Phänomene genetischer Instabilität zu erforschen. Ziel ist, neue prognostische Prädiktoren zu entwickeln, die es erlauben, klonale Evolution frühzeitig zu erkennen, messbar zu machen und neue Zielstrukturen für zukünftige Therapien zu identifizieren.


PD Dr. Wolfgang Seifarth
Telefon 0621/383-71302
Telefax 0621/383-71331
wolfgang.seifarth@
medma.uni-heidelberg.de
Prof. Dr. Alice Fabarius
Telefon 0621/383-71307
Telefax 0621/383-71329
alice.fabarius@
medma.uni-heidelberg.de
Helga Kleiner
BTLA/Dipl.-Ing. Biotech. (FH)
Nicole Naumann
M.Sc., Dr. sc. hum.